Introducción
El principio de exclusión de Pauli sólo es aplicable a fermiones, esto es, partículas que forman estados cuánticos antisimétricos y que tienen espín semientero. Son fermiones, por ejemplo, los electrones y los quarks (estos últimos son los que forman los protones y los neutrones). El principio de exclusión de Pauli rige, así pues, muchas de las características distintivas de la materia. En cambio, partículas como el fotón y el (hipotético) gravitón no obedecen a este principio, ya que son bosones, esto es, forman estados cuánticos simétricos y tienen espín entero. Como consecuencia, una multitud de fotones puede estar en un mismo estado cuántico de partícula, como en los láseres.
Es sencillo derivar el principio de Pauli, basándonos en el teorema espín-estadística aplicado a partículas idénticas. Los fermiones de la misma especie forman sistemas con estados totalmente antisimétricos, lo que para el caso de dos partículas significa que:
(La permutación de una partícula por otra invierte el signo de la función que describe al sistema). Si las dos partículas ocupan el mismo estado cuántico 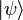 , el estado del sistema completo es
, el estado del sistema completo es  . Entonces,
. Entonces,
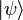 , el estado del sistema completo es
, el estado del sistema completo es  . Entonces,
. Entonces,
así que este caso no puede darse porque en ese caso el ket anterior no representa un estado físico. Este resultado puede generalizar por inducción al caso de más de dos partículas.
[editar]Consecuencias
El caso más conocido por su amplia utilización en el campo de la química y la física átomica es en el sistema cuántico del átomo de Schrödinger siendo los fermiones los electrones. Por ello es la versión más conocida de este lema: "Dos electrones en la corteza de un átomo no pueden tener al mismo tiempo los mismos números cuánticos". Esto explica que los electrones se distribuyan en capas alrededor de un núcleo y que por tanto los átomos con más electrones ocupen un tamaño mayor, además de que no sea posible interpenetrar de cierta manera las nubes electrónicas de los átomos, este hecho explica de hecho la impenetrabilidad de la materia ordinaria macroscópica.
Otro fenómeno físico del que es responsable el principio de Pauli es el ferromagnetismo, en el que el principio de exclusión implica una energía de intercambio que induce al alineamiento paralelo de electrones vecinos (que clásicamente se alinearían antiparalelamente).

No hay comentarios:
Publicar un comentario